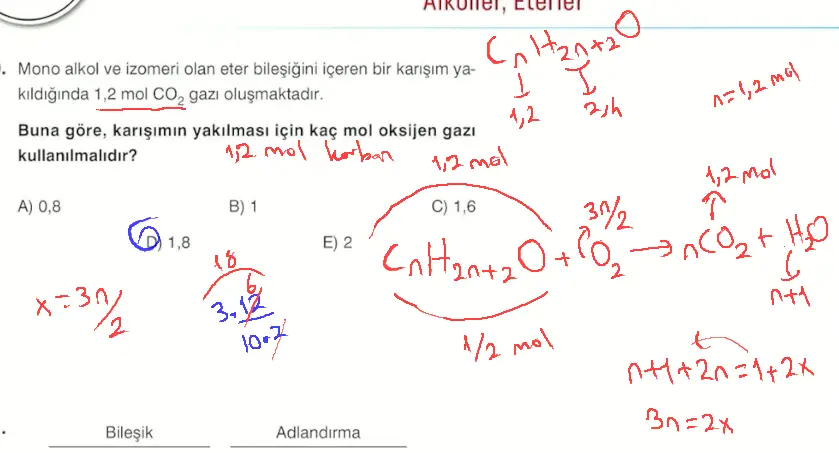
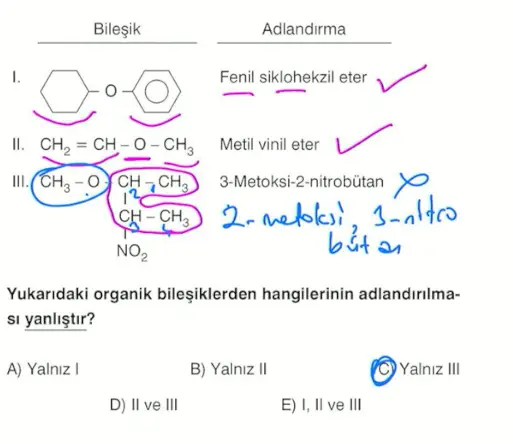
Eterler
Genel yapıları \(R-O-R\) şeklindedir.
- İki kez alkillenmiş su olarak tanımlanabilirler.
- Düz zincirli veya halkalı yapıda olabilirler.
- Düz zincirli eterlerin genel formülü \(C_nH_{2n+2}O\) dur.
- Eterler, oksijene bağlı yan gruplar aynı ise simetrik (basit) eter, gruplar farklı ise asimetrik (karışık) eter olarak sınıflandırılır.

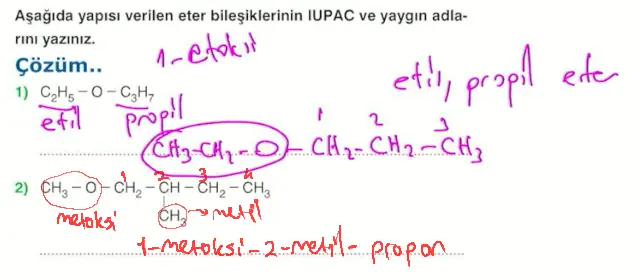
Eterlerin IUPAC Sistemine Göre Adlandırılması
Oksijene bağlı en uzun karbon zinciri seçilerek numaralandırılır.
Karbon sayısı az olan kısım oksijen ile birlikte alkoksi \((-OR)\) grubunu oluşturur. Karbonlara numara verilirken alkoksi \((RO-)\) grubuna yakın uçtan başlanır.
- Alkoksi grubunda alkanın isminin sonundaki -an eki yerine -oksi eki getirilerek alkoksi grubunun ismi bulunur.
Bileşik adlandırılırken alkoksi grubunun yeri ve adı belirtilerek ana zincirdeki C sayısına karşılık gelen hidrokarbonun adı söylenir.
Eterlerin yaygın adlandırılmasında oksijene bağlı radikal gruplarının adı alfabetik sırayla yazılır ve sonuna eter sözcüğü getirilir.
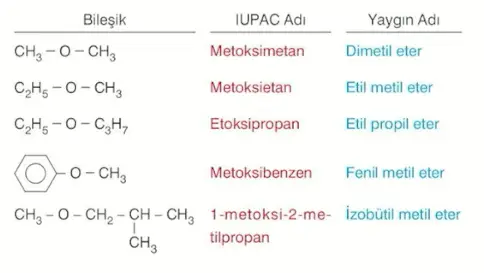
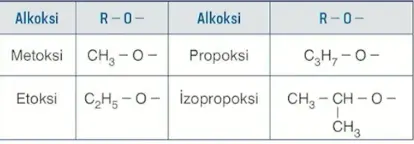
Eterlerin Fiziksel Özellikleri
- Eterlerin molekül geometrileri su ve alkol bileşikleri gibi açısaldır.
- Eterler renksizdir ve kendilerine özgü kokuları vardır.
- Polar yapılı bileşiklerdir.
- Yoğunlukları genellikle souyun yoğunluğundan küçüktür.
- Eter molekülleri arasında hidrojen bağı yoktur. Ancak eter molekülündeki oksijen atomunun ortaklanmamış elektron çiftiyle su molekülündeki hidrojen atomu arasında moleküller arası hidrojen bağı oluşur. Bu nedenle az karbonluları suda çözünürler.
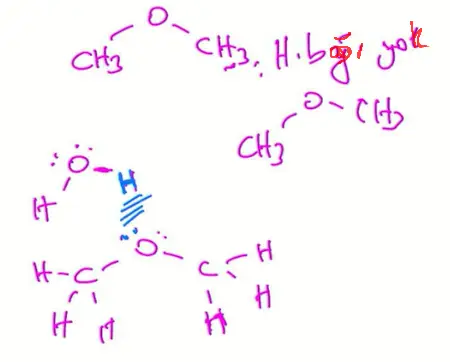
- Kaynama noktaları aynı karbon sayılı alkollere göre düşüktür.
- Karbon sayıları arttıkça sudaki çözünürlükleri azalır.
- Eterler; kimyasal tepkimelere karşı oldukça ilgisiz (inert) bileşiklerdir. Organik bileşikler için iyi bir çözücü ve inert olmalarından dolayı, organik bileşiklerin özütlenmesinde ve bazı kimyasal tepkime ortamlarında çözücü sıvısı olarak kullanılırlar.
Eterlerin Eldeleri
2 mol monoalkolden \(140\degree C\) de asit katalizörlüğünde 1 mol su çekilmesiyle eterler oluşur.
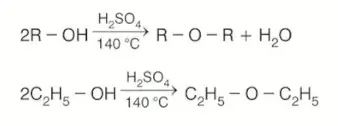
Eterlerin Kimyasal Tepkimeleri
Eterler yanıcılığı yüksek olan bileşiklerdir.
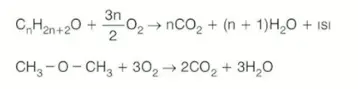
Laboratuvarda eterle çalışılıyorsa yakınında bek alevi olmamalıdır.
Eterler Laboratuvarlarda açık bırakılmamalıdır. Çünkü bazı eterler havadaki oksijenle etkileşerek patlayıcı özelliğe sahip peroksitleri oluşturur. Bu nedenle laboratuvarda eterle çalışılacaksa oluşan peroksit ortamdan mutlaka uzaklaştırılmalıdır.
Eterlerin Kullanım Alanları
Eterler çoğunlukla kimya ve tıp alanında kullanılır.
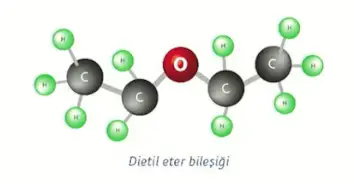
- Dietileterin (lokman ruhu) kaslar üzerinde gevşetici etkisi vardır. Bu nedenle eskiden anestezik olarak kullanılmıştır. Ancak dietileter; nabzı, solunumu ve kan basıncını etkiler, solunum yollarını tahriş eder, mide bulantısı yaparak kusmaya sebep olur. Bu yan etkilerinden dolayı eterlerin anestezide kullanımından vazgeçilmiştir.
- ter-Bütil metil eter, sanayide MTBE diye adlandırılır ve benzinin oktan sayısını artırmak için kullanılır. Depolanması ve taşınması esnasında çevre kirliliğine sebep olma ihtimalinden dolayı son zamanlarda kullanımından vazgeçilmiştir.
Alkol-Eter İzomerliği
Aynı karbon sayılı monoalkoller ile eterler fonksiyonel grup izomeridir.
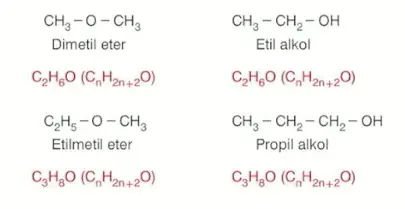
Bir karbonlu alkolün eter izomeri yoktur.
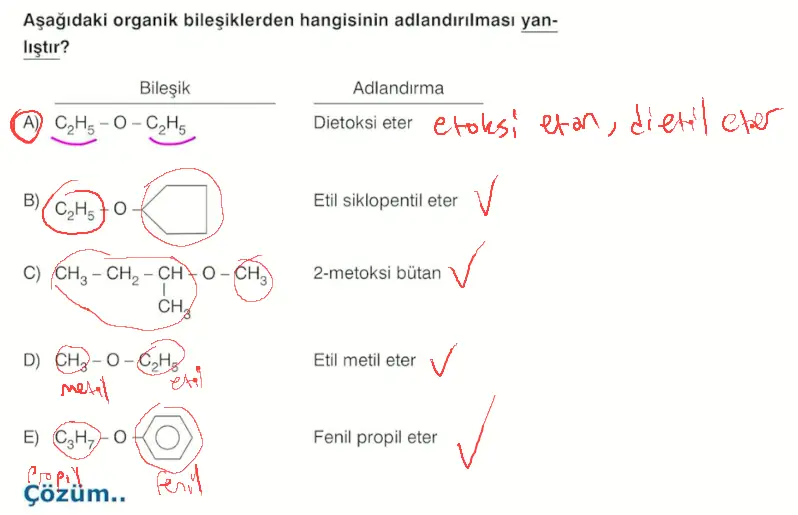
Questions
- İkincinin özel adı: izopentil metil eter
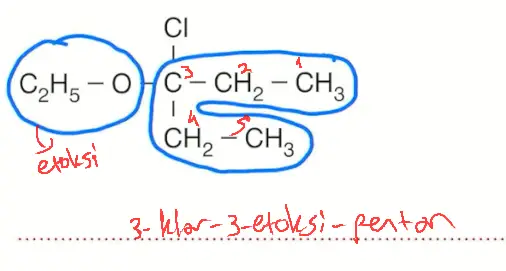


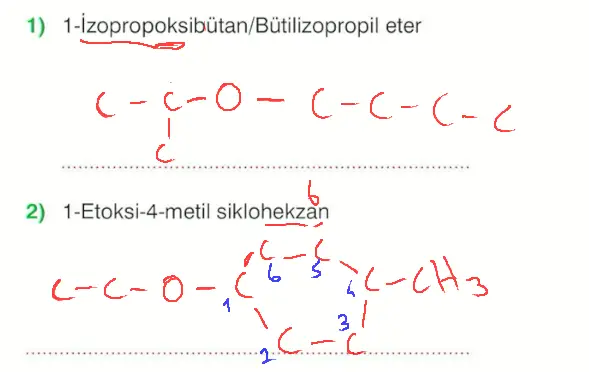

- Sadece C ve H dan oluşan bileşikler apolardır. Suda iyi çözünmez.
- Alkol polar olduğu için suda diğerlerinden daha iyi çözünür.

- Eğer OH'ın bağlı olduğu karbonda pi bağı varsa molekül kararsızdır.
- OH'ın bağlı olduğu atomda pi bağı varsa o alkol değildir.