Alkoller
Genel gösterimleri \(R-OH\) dir. Alkollerde fonksiyonel grup hidroksil \((-OH)\) grubudur.
\(sp^3\) hibritleşmesi yapmış karbon atomuna \(-OH\) grubunun bağlanmasıyla oluşur.
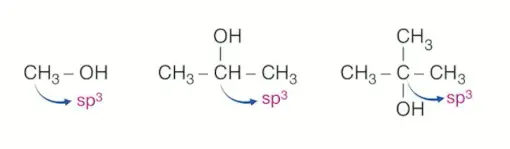
\(-OH\) grubunun bağlı olduğu karbon atomu pi bağı içeriyorsa ALKOL DEĞİLDİR.
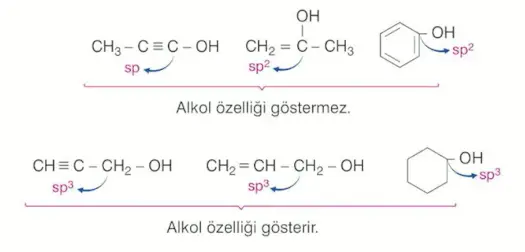
\(-OH\) grubunun bağlı olduğu karbon atomuna başka bir \(-OH\) grubu veya farklı bir fonksiyonel grup bağlı olan bileşikler ALKOL DEĞİLDİR.
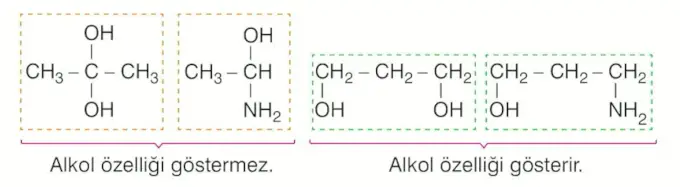
Alkollerin Sınıflandırılması
Alkoller içerdikleri \(-OH\) grubu sayısına göre; monoalkol ve polialkol, \(-OH\) grubunun bağlı olduğu karbon atomunun durumuna göre; primer, sekonder ve tersiyer olarak sınıflandırılır.
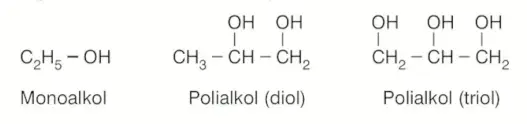
- Yapısında 1 tane \(-OH\) grubu bulunan alkollere monoalkol denir.
- Monoalkollerin genel formülü \(C_nH_{2n+2}O\) dur.
- Yapısında farklı karbon atomlarında 1 den fazla \(-OH\) grubu içeren alkollere polialkol denir.
2 tane \(-OH\) grubu içeren alkollere dialkol (diol), 3 tane \(-OH\) grubu içeren alkollere trialkol (triol) denir.
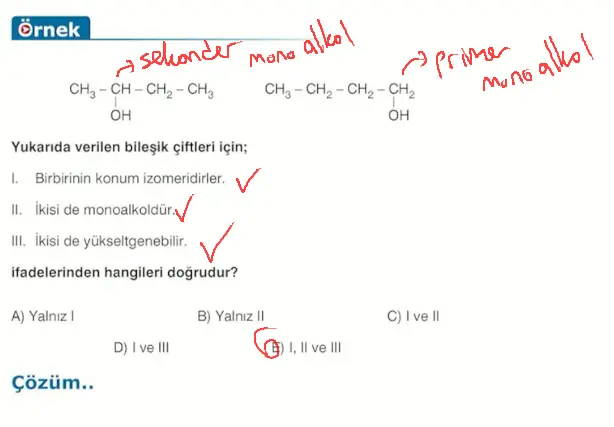
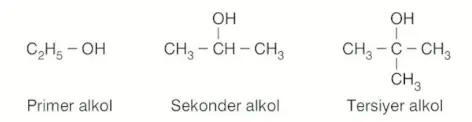
\(-OH\) grubunun bağlı olduğu karbon atomunun 1 tane karbon atomuna bağlı olduğu alkollere primer (birincil) alkol denir. (\(CH_3OH\) bileşiği de primer alkoldür.)
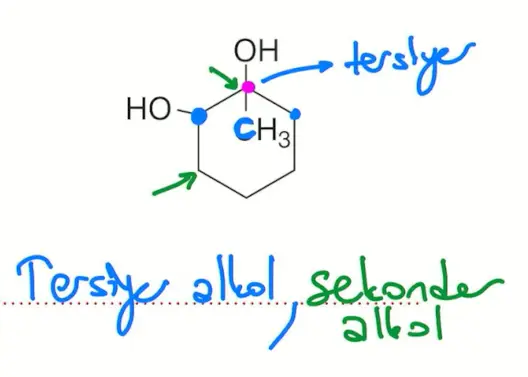
\(-OH\) grubunun bağlı olduğu karbon atomunun 2 tane karbon atomuna bağlı olduğu alkollere sekonder (ikincil) alkol denir.
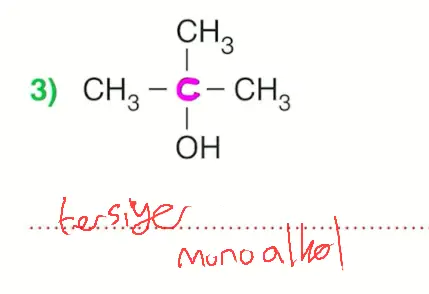
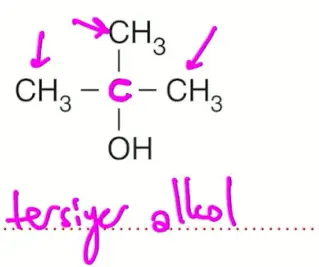
\(-OH\) grubunun bağlı olduğu karbon atomunun 3 tane karbon atomuna bağlı olduğu alkollere tersiyer (üçüncül) alkol denir.
Alkollerde hidroksil grubunun bağlı olduğu karbon atomu \(\alpha\) (alfa) karbon atomu olarak adlandırılır.
Alkollerin IUPAC Sistemine Göre Adlandırılması
Hidroksil grubunu içeren en uzun karbon zinciri seçilir.
- Hidroksil grubuna en yakın uçtan başlanarak zincirdeki karbon atomları numaralandırılır.
Zincirdeki alkil gruplarının ve heteroatomların yeri ve adı belirtilir.
Hidroksil grubunun yeri belirtilerek zincirdeki karbon sayısına göre alkan adlandırılması yapılır ve alkanın adının sonuna -ol eki getirilir.
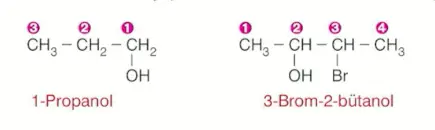
İkili ve üçlü bağ, hatta alfabetik öncelik diğer uçta olsa bile öncelik OH'ların numaraları toplamının en küçük olmasıdır.
Bileşik birden fazla hidroksil grubu içeriyorsa bu grupların yerleri belirtilerek adlandırmadaki -ol ekinin önüne hidroksil grubu sayısına göre di-, tri-, tetra- gibi ekler getirilir.
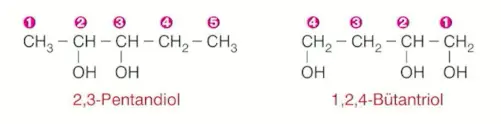
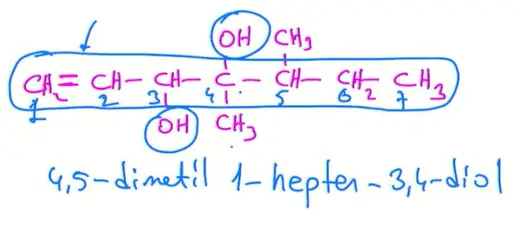
İkili ya da üçlü bağ içeren doymamış alkol molekülleri adlandırılırken \(-OH\) grubunun bağlı olduğu karbona küçük numara gelecek şekilde numara verilir ve ikili ya da üçlü bağların yerleri belirtilir.
- Zincirdeki karbon sayısına göre doymamış hidrokarbonun adından sonra hidroksil grubunun yeri belirtilip -ol eki getirilir.
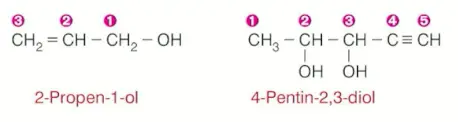
Alkollerin yaygın adlandırılması yapılırken hidroksil grubunun bağlı olduğu alkil grubunun adından sonra alkol kelimesi getirilir.
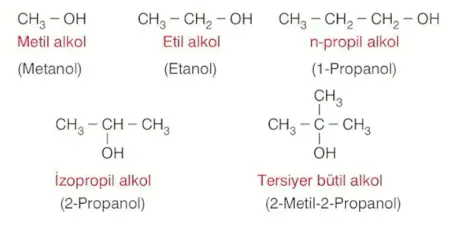
IUPAC adlandırmasında zincirin hidrojen eksilmemiş isminin (alkil değil alkan) sonuna -ol eki getirilir.
Alkollerin Fiziksel Özellikleri
Alkoller \(-OH\) grubundan dolayı hidrojen bağı içerirler ve polardırlar. Bu nedenle kaynama noktaları aynı karbon sayılı hidrokarbonlardan büyüktür.
Monoalkollerde karbon sayısı arttıkça kaynama noktası artar.
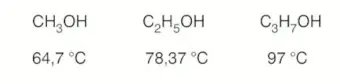
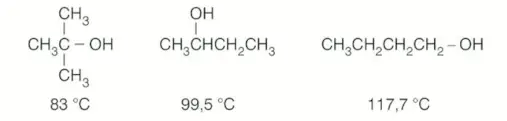
Aynı sayıda karbon taşıyan alkollerde dallanma arttıkça kaynama noktası düşer.
- Aynı karbon sayılı alkollerde tersiyer alkolün kaynama noktası en düşük, primer alkolün kaynama noktası en yüksektir.
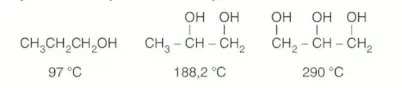
Alkollerin yapısındaki \(-OH\) grubu sayısı arttıkça hidrojen bağı sayısı artar ve kaynama noktaları yükselir.
Alkollerde karbon zinciri apolar, \(-OH\) grubu ise polar yapıya sahiptir.
- Karon zincirleri uzadıkça hidrofob özellikleri artar ve buna bağlı olarak sudaki çözünürlükleri azalır.
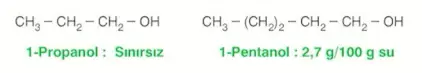
Alkolün \(-OH\) grubu sayısı arttıkça sudaki çözünürlüğü artar.
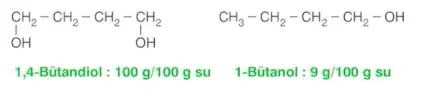
Alkoller homolog sıra oluştururlar.
Önemli Alkoller
Metanol (Metil Alkol)
- Alkollerin en basit üyesidir.
- Kaynama noktası \(64,7\degree C\) olup, açık mavi alevle yanar.
- Odunun havasız ortamda ve yüksek sıcaklıkta damıtılmasıyla elde edildiğinden metanole "odun alkolü" de denilmektedir.
- Çok zehirlidir; az miktarda yutulması körlüğe, çok miktarda yutulması ölüme yol açabilir. Beyine ciddi derecede hasar verir.
- Buharının solunmasıyla da metanol zehirlenmesi meydana gelebilir.
- Metanol araçlarda yakıt olarak da kullanılabildiğinden alternatif yakıt olarak kullanılması amacıyla çalışmalar yapılmaktadır.
Etanol (Etil Alkol)
- Çok yaygın bir kullanım alanına sahiptir.
- Normal kaynama noktası \(78\degree C\) dir.
- Şekerin fermantasyonuyla elde edilebilir. Fermantasyon genellikle suyla şeker karışımına maya katılarak yapılır. Maya; içerdiği enzimlerle şekeri, etanol ve karbondiokside dönüştürür.
- \(\ce{C6H12O6 ->[Maya] 2C2H5OH + 2CO2}\)
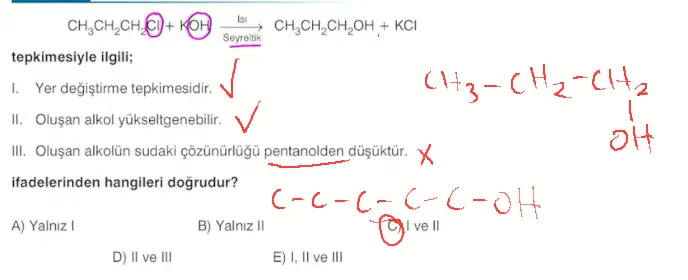
- Etanol, alkil halojenürlerin seyreltik NaOH ya da KOH çözeltileri ile tepkimesinden de elde edilebilir. Bu tepkimede alkil halojenürdeki halojen ile NaOH ya da KOH çözeltisindeki hidroksil iyonu yer değiştirerek etanol elde edilir.
- \(\ce{CH3-CH2-Cl + KOH ->[Heat][Seyreltik] CH3-CH2-OH + KCl}\)
- \(\ce{CH3-CH2-Cl + NaOH ->[Heat][Seyreltik] CH3-CH2-OH-NaCl}\)
- Endüstri için de önemli bir kimyasal olan etanol etenin asidik ortamda su ile tepkimesinden elde edilir.
- \(\ce{CH2=CH2 + H2O ->[Acid] CH3-CH2-OH}\)
- Etanol; çeşitli bitkilerin fermantasyonutla üretilebildiği için aynı zamanda yenilenebilir bir enerji kaynağıdır. Etanol elde edildikten sonra benzinle çeşitli oranlarda karıştırılarak kullanılabilir. Ancak etanol, benzine göre daha düşük enerjiye sahiptir.
- Etanol, sağlık alanında lokal antiseptik olarak kullanılmaktadır.
- İyi bir çözücü olan etanol ilaç yapımında, parfüm ve kolonya üretiminde kullanılmaktadır.
Alkolerin Eldeleri
Etil alkolün eldesinde kullanıllan bazı yöntemler genel olarak alkollerin eldesinde kullanılabilir.
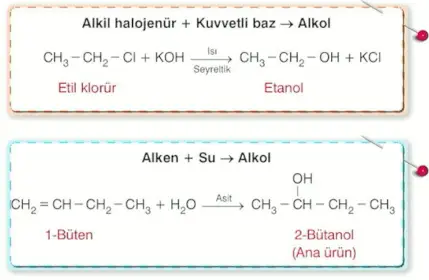
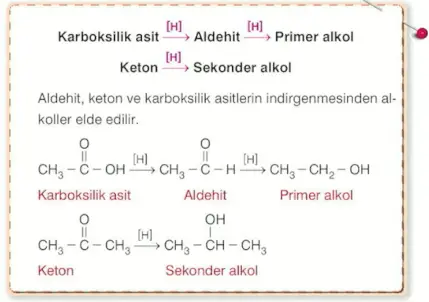
[H] ifadesi bir derece indirgenme anlamındadır.
Organik bileşiklerin indirgenme ve yükseltgenmelerinde yaygın bazı indirgen ve yükseltgenler kullanılır.
- \(LiAlH_4\) ve \(NaBH_4\) yaygın kullanılan indirgen maddelerdir.
- Hidrojen atomları fazladır.
- \(KMnO_4\) ve \(K_2Cr_2O_7\) yaygın kullanılan yükseltgen maddelerdir.
- Oksijen atomları fazladır.
Yükseltgenme kısaca \(\ce{->[(O)]}\) şeklinde gösterilir. Molekülden bir hidrojen çıkarmayı ifade eder.
İndirgenme tepkimeleri kısaca \(\ce{->[(H)]}\) şeklinde gösterilir.
Alkollerin Kimyasal Tepkimeleri
Yanma Tepkimeleri
Alkollerin yanma tepkimeleri sonucunda \(CO_2\) ve \(H_2O\) oluşur.
\[\ce{CnH_{n+2}O + \frac{3n}{2}O2 -> nCO2 + (n+1)H2O + Heat} \]
Kondenzasyon Tepkimeleri
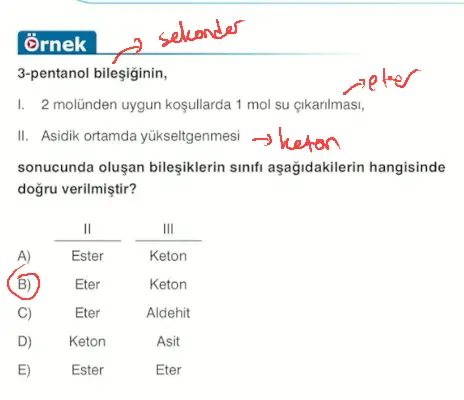
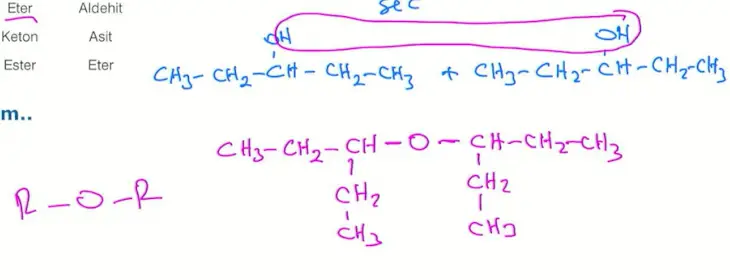
2 mol monoalkolden 1 mol su çekilmesiyle eterler oluşur.
\[2R-OH ->[H_2SO_4][140\degree C] R-O-R + H2O \]
1 mol alkolden 1 mol su çekilirse alken meydana gelir.
Karboksilik asitler ile alkollerin tepkimesinden esterler oluşur.
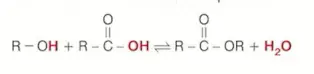
Yükseltgenme Tepkimeleri
Alkollerin yükseltgenmesi, alkolün primer, sekonder veya tersiyer olmasıyla ilgilidir.
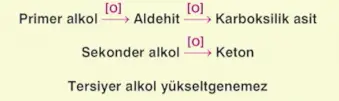
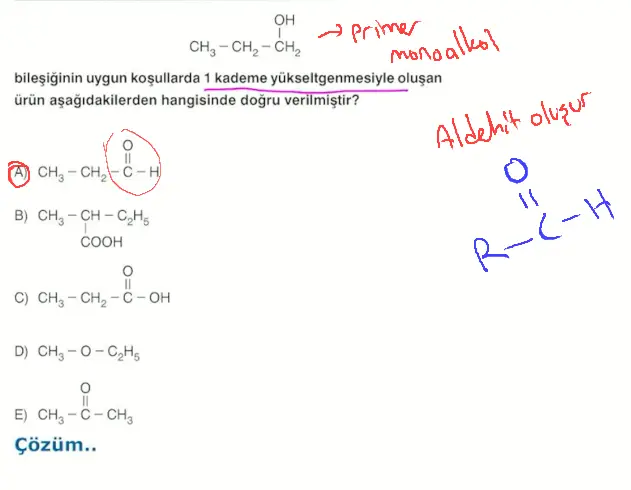
- Primer alkolde, OH'ın bağlı olduğu karbona 2 adet H bağlıdır. Bu da 2 kez yükseltgenebilmesini sağlar.
- Sekonder alkolde bir tane H bağlıdır. Bu da bir kez yükseltgenebildiği anlamına gelir.
- Tersiyer alkolde OH'ın bağlı olduğu karbona H bağlı olmadığı için yükseltgenemez.
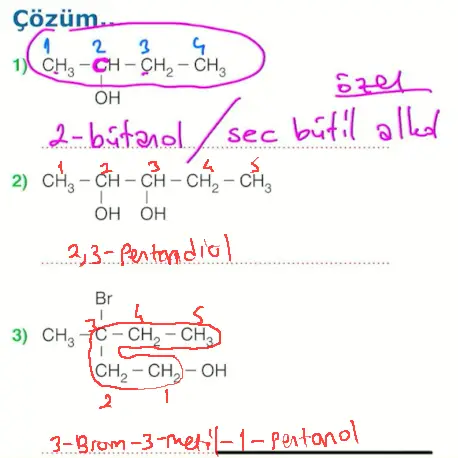
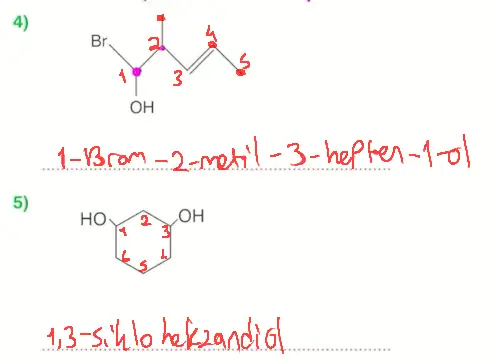
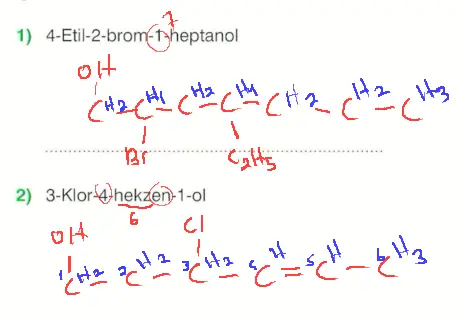
Questions
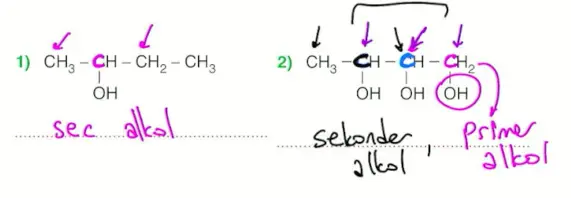

- Alkoldeki karbon zinciri uzadıkça (yüzey alanı arttığı için) ve OH sayısı arttıkça (hidrojen bağı sayısı arttığı için) kaynama noktası yükselir.
- En uzun zincire ve en çok OH'a sahip madde ise B şıkkındadır.