Alkinler (Asetilenler)
Yapısında en az bir tane üçlü bağ bulunduran hidrokarbonlara alkin (monoalkin), yapısında birden fazla üçlü bağ bulunduran alkinlere polialkin denir.
Alkinler yapısında üçlü bağ bulundurduğundan en az iki tane pi bağı içerir. Bu nedenle doymamış hidrokarbonlardır.
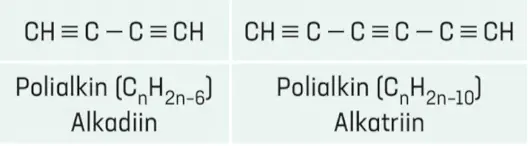
Düz zincirli monoalkinlerin genel formülü \(C_nH_{2n-2}\) dir.
- Çünkü her bir pi bağı \(C_nH_{2n+2}\) formülünden iki hidrojen azaltır.
Alkinlerin Adlandırılması
Adlandırmada seçilen ana karbon zinciri üçlü bağlı karbonları içerecek şekilde seçilir.
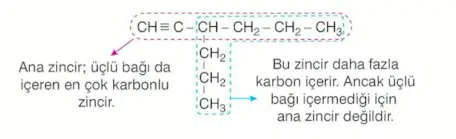
Üçlü bağın yakın olduğu uçtan başlanarak karbon atomlarına numara verilir.
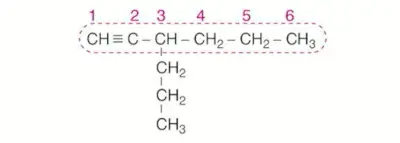
Üçlü bağ her iki uca eşit mesafede ise önce dallanma, sonra alfabetik önceliğe bakılır.
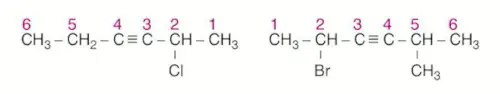
Bileşikteki yan grupları adlandırma işlemi alkanlardaki kurallara göre yapılır.
- Yan grupların adları yazıldıktan sonra üçlü bağın bulunduğu karbon numarası yazılır ve ana zincirdeki karbon sayısına eşit karbonlu alkanın adının sonundaki -an yerine -in eki getirilerek adlandırma yapılır.
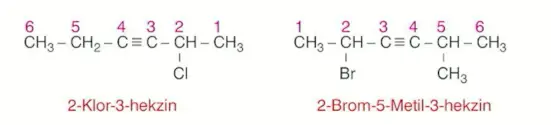
2 ve 3 karbonlu alkinlerde üçlü bağın yerini belirtmeye gerek yoktur.
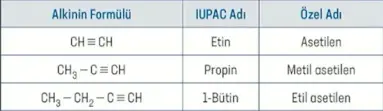
Alkinin yapısında birden fazla üçlü bağ varsa, C atomları üçlü bağlara yakın uçtan numaralandırılır. Üçlü bağ sayısının bulunduğu karbon atomu numarası belirtildikten sonra üçlü bağ sayısı -diin, -triin gibi eklerle belirtilir.
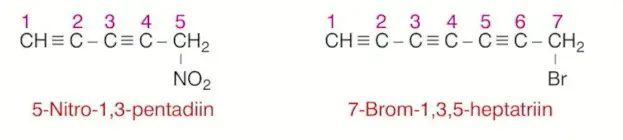
Alkinlerden 1 hidrojen çıkarılmasıyla oluşan radikallere alkinil denir. Bu gruplar adlandırılırken alkin adının sonuna -il eki getirilir.
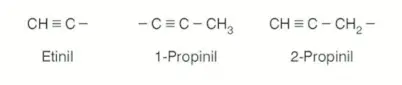
Radikallerde numaralandırılmaya açık karbondan başlanır.
THE BELOW IS IMPORTANT
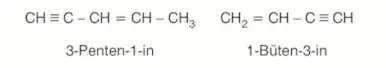
Molekülde hem ikili hem de üçlü bağ varsa ve bu bağlar zincir uçlarına eşit uzaklıkta ise C atomlarının numaralandırılması ikili bağın olduğu taraftan yapılır.
Eğer farklı uzaklıkta iseler, çoklu bağların yakın olduğu uçtan numaralandırma yapılır.
- Ana zincir alken adıyla okunur.
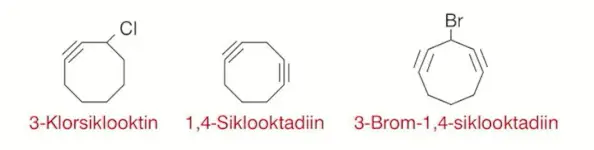
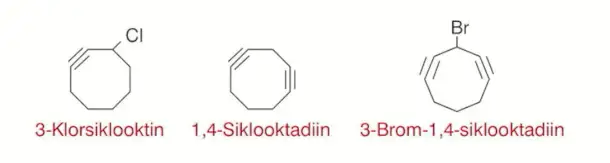
Halkalı yapıdaki alkinler sikloalkin olarak adlandırılır. Halkadaki C atomlarının numaralandırılması üçlü bağ karbon atomlarına 1 ve 2 numara verilerek yapılır. Üçlü bağ 1 tane ise yeri belirtilmez. Üçlü bağ sayısı 1 den fazla ise yerleri belirtilir.
Alkinlerin Özel Adlandırması
Alkinlerin özel adlandırılması asetilene göre yapılır. Aralarında üçlü bağ bulunan karbon atomları (asetilen) merkez kabul edilir.
Bu merkeze bağlı gruplar alfabetik sıraya göre yazılır ve sonuna asetilen kelimesi getirilir.
Alkinlerin Genel Özellikleri
- Apolar yapılıdırlar ve suda çözünmezler.
- Moleküller arasında London kuvvetleri etkindir. Karbon sayısı azaldıkça ve dallanma arttıkça kaynama noktaları düşer.
- Homolog sıra oluştururlar.
- En az iki tane pi bağı ve sp hibritleşmesi yapmış C atomu içerirler.
Alkinlerin Kullanım Alanları
Asetilen oda koşullarında gaz halinde olan bir bileşiktir. Çok çabuk alev alabildiği ve yüksek derecede ısı vererek yandığı için metallerin kesilmesinde ve kaynak işleminde kullanılır.
Asetilen gazı çok kararsız bir yapıya sahiptir. Yüksek basınca maruz kaldığında patlar. Bu nedenle saf asetilen gazının yüksek basınç ile sıvılaştırılması tehlikelidir.
Asetilen endüstride aşağıdaki zincirleme tepkimelerle elde edilir.

Alkinlerin Kimyasal Tepkimeleri
Yanma Tepkimesi
Alkinlerin genel yanma tepkimeleri aşağıdaki gibidir.
\[\ce{C_nH_{2n-2} + \frac{3n-1}{2}O2 -> nCO2 + (n-1)H2O + Heat} \]
Katılma Tepkimeleri
Halojen Katılması (Halojenasyon)
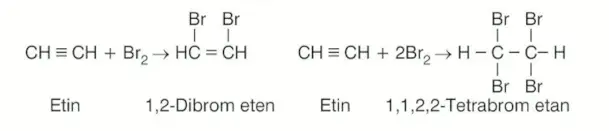
Alkinlere halojenler katılabilir. Halojenlerden \(Br_2\) ile tepkimeleri, bromlu suyun rengini giderme olarak adlandırılır. Tepkime sonucunda haloalkan bileşiği oluşur.
Hidrojen Katılması (Hidrojenasyon)
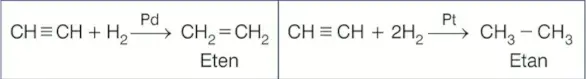
Alkinlere yüksek basınçta, katalizörlerle birlikte \(H_2\) katıldığında alken veya alkana dönüşürler.
- Örneğin asetilene palladyum (Pd) kalatizörlüğünde 1 mol \(H_2\) katılırsa alken,
- Platin (Pt) katalizorlüğünde 2 mol \(H_2\) katılırsa alkan elde edilir.
Hidrojen Halojenür Katılması (Hidrohalojenasyon)
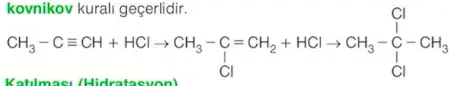
Alkinlere hidrojen halojenür (HX) bileşiğinin katılmasında alkinin üçlü bağlı karbonları özdeş değilse alkenlerde olduğu gibi Markovnikov kuralı geçerlidir.
Su Katılması (Hidratasyon)
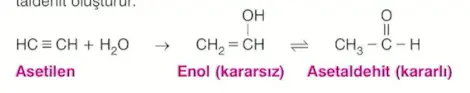
Asetilen, su ile katılma tepkimesi vererek önce kararsız bir bileşik olan enol, sonra denge tepkimesiyle kararlı bir bileşik olan asetaldehit oluşur.
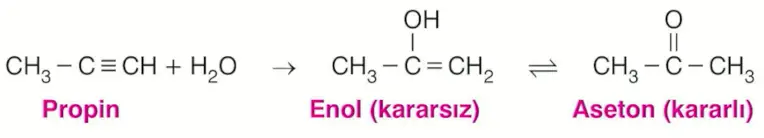
Karbon sayısı 3 ve daha fazla olan alkinlere su katılırsa önce kararsız bir bileşik olan enol, sonra denge tepkimesiyle kararlı bir bileşik olan keton (\(C_nH_{2n}O\)) oluşur.
Polimerleşme Tepkimeleri
Alkinler pi bağı içerdiğinden polimerleşme tepkimesi verir.
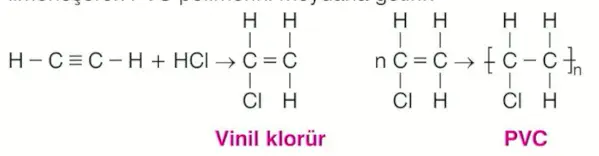
Asetilene HCl katılması sonucunda oluşan vinil klorür bileşiği polimerleşerek PVC polimerini meydana getirir.
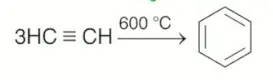
3 mol asetilenin \(600\degree C\) de trimerleşmesinden benzen elde edilir.
Yer Değiştirme Tepkimeleri
Üçlü bağın 1. ve 2. karbon atomları arasında olduğu alkinler (yani üçlü bağlı karbonların en az birinde H atomu olan alkinler) uç alkin, 1. ve 2. den farklı karbon atomları arasında olduğu alkinler ise (yani üçlü bağlı karbonlarda H atomu olmayan alkinler) iç alkin olarak adlandırılır.
- Uç alkin örnekleri: \(HC\equiv CH, CH_3-C\equiv CH, CH_3-CH_2-C\equiv CH\)
- İç alkin örneği: \(CH_3-CH_2-C\equiv C-CH_3\)
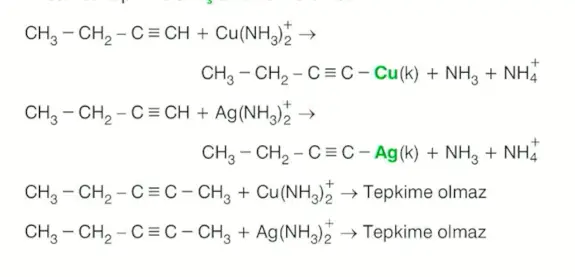
Asetilen, amonyaklı \(AgNO_3\) çözeltisiyle (Tollens ayıracı) tepkime vererek beyaz çökelek oluşturur.

Uç alkindeki gümüş ile hidrojen yer değiştirir.
Üçlü bağın olduğu karbonda hidrojen yoksa yer değiştirme tepkimesi gerçekleşmez. (Uç alkin değil ise, iç alkin ise)
Asetilen, amonyaklı \(CuNO_3\) çözeltisiyle (Fehling ayıracı) tepkime vererek kırmızı çökelek oluşturur.
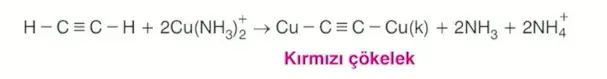
Aseetilen bileşiğinin Fehling ve Tollens ayıraçlarıyla yer değiştirme tepkimesi vererek oluşturduğu metal asetilenür tuzları darbelere karşı dayanıksızdır ve patlayıcı özellik gösterirler.
Asetilenin verdiği yukarıdaki tepkimeleri tün uç alkinler verebilir. Ancak bu tepkimeleri iç alkinler veremez.
Questions
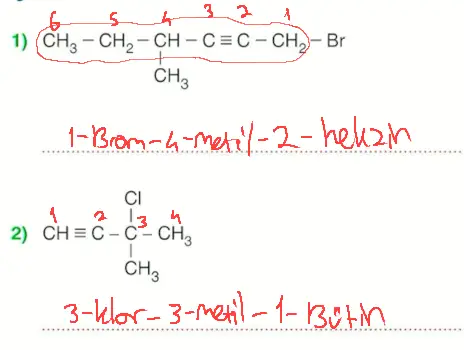
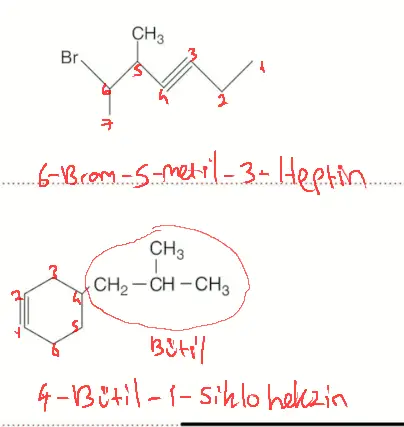
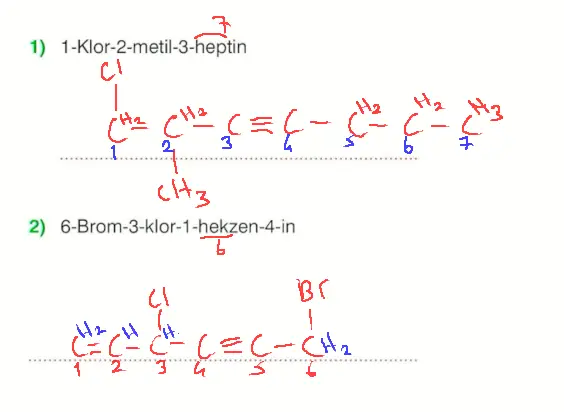

- Bu soruyu tekrar çöz.

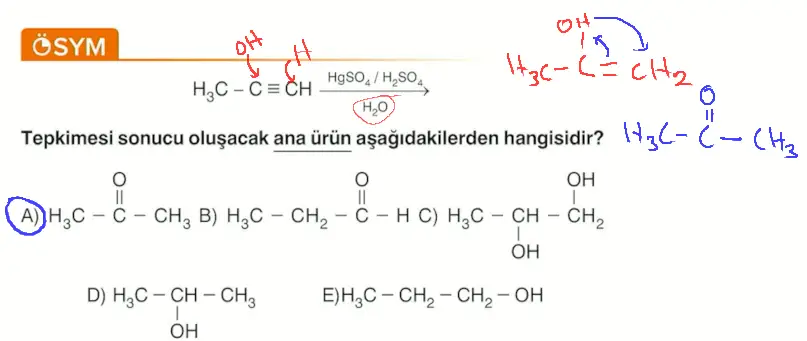





- Propin sınırlayıcı bileşendir. Sudan yeterli miktarda vardır.
- Denge tepkimesi olduğundan ketondan daha az oluşmaz mı? Sanırım bunu görmezden geliyoruz? Evet, öyle olmalı.

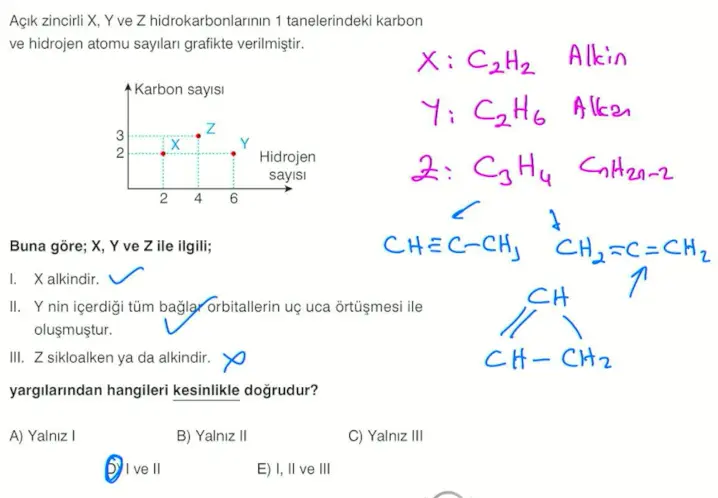
- Açık zincirli ne demek?

- 0,1 molde 0,5 mol CO2 oluşuyorsa molekülde 5 adet karbon vardır.

- Sorude atomların mol kütlelerini vermediği için karışımın toplam kütlesi hesaplanamaz.
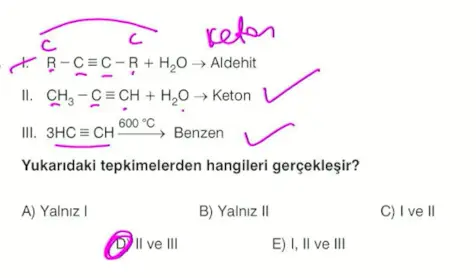
- R: Radikal anlamındadır.